导读:截至1月31日,国家药监局已应急审批7个新型冠状病毒核酸检测试剂,部分产品仅用4天走完流程,再显中国速度!2月1日,工信部相关负责人介绍,新型冠状病毒核酸检测试剂日产量已经达到了77.3万人份......
作者:Linan
7个检测产品通过国家药监局应急审批
1月26日,国家药监局发文称应急审批新型冠状病毒核酸检测试剂,全力服务疫情防控需要。内容提到,应急审批已通过4家企业4个新型冠状病毒检测产品。此后,国家药监局又分别于28日、31日先后共批准6家新型冠状病毒试剂盒生产企业的产品上市,分别是华大基因、上海之江、上海捷诺、圣湘生物、达安基因、上海伯杰医疗。

截至31日,国家药监局共应急审批了6家企业7个新型冠状病毒核酸检测试剂。国家药监局表示将根据疫情防控需要,继续做好相应产品应急审批工作。
新型冠状病毒检测试剂应急审批情况
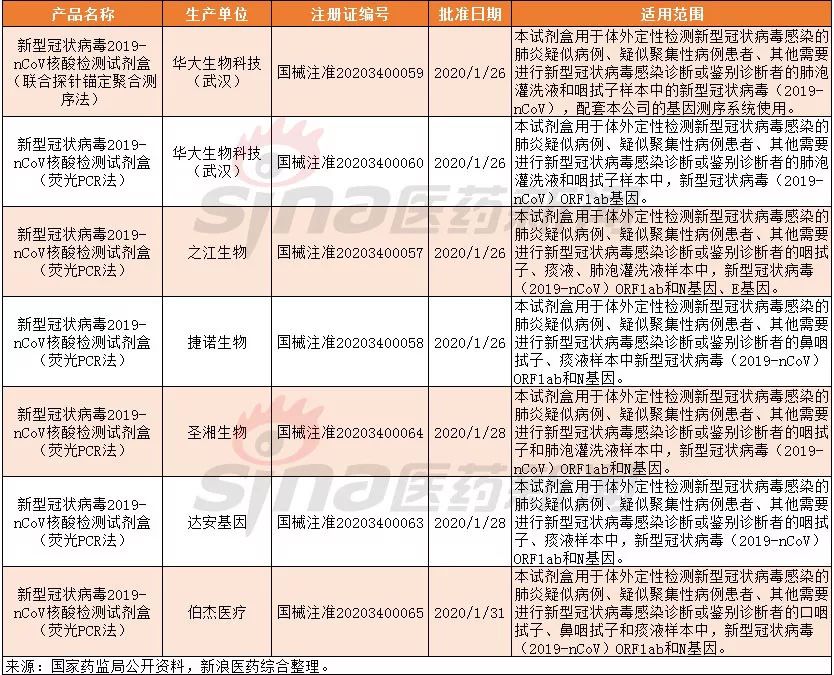
据相关报道,新冠病毒试剂盒这种与致病性病原体抗原、抗体以及核酸等检测相关的试剂,按国家法规,属于体外诊断试剂的第三类,也就是医疗器械中的最高审查级别,需要由国家食品药品监督管理总局审查,因此审查程序也繁琐漫长。分析人士指出,按照常规流程,体外分子诊断产品走进医院市场需经过2-3年的临床试验。而此次国家药监局开辟绿色通道,仅用4天就走完流程。
行业人士指出,以往这类证件的有效期一般是5年,但此次国家药监局应急审批通过的注册证有效期都为1年,注册信息中还强调,该产品仅为新冠病毒感染的肺炎的辅助诊断及应急储备,另企业应当在延续时按照医疗器械注册管理办法的要求完善所有注册申报资料等信息。
另一边,在通过应急审批之后,华大基因、圣湘生物、达安基因等都竭力扩大生产,保障市场供应。例如,日前华大基因已完成约30万人份的新型冠状病毒检测试剂盒生产,极大缓解了试剂盒供应压力,日均产能已达8万人份,同时已继续安排增加生产30万人份试剂盒,新储备30万人份试剂盒原料;圣湘生物相关人士表示,面对突发疫情应急物资短缺的需求,公司春节假期紧急调配员工返岗,组织研发生产,所有生产线满负荷工作,新型冠状病毒核酸检测试剂日均产能最高可达50万人份;而达安基因日前亦有透露,目前该试剂盒110分钟左右可出结果,日均可生产20万人份,后续可达50万人份/日,核心原材料均为达安基因自身所掌握。该公司负责人表示,已做好全力以赴保障市场供应的准备,且公司产能完全能够满足市场的需求。
多家企业公布检测试剂研究进展
值得一提的是,1月10日,新型冠状病毒的基因组序列被测出并对外公布。1月26日,国家基因组科学数据中心首次公开新型冠状病毒全基因组序列,病毒基因组序列的公布为新型冠状病毒核酸检测试剂盒的开发迎来时间窗口。
除上述企业之外,国家多家企业都在布局研发新型冠状病毒核酸检测试剂,具体如下:
硕世生物
硕世生物基于荧光PCR的技术,于2020年1月13日开发了新型冠状病毒核酸检测试剂盒以及冠状病毒通用型核酸检测试剂盒。1月28日,硕世生物新型冠状病毒检测试剂在江苏省医疗器械检验所完成所有项目的检验,符合产品技术要求。成为江苏省法定检验机构检定合格的第一个新型冠状病毒检测试剂。
热景生物
为应对新型冠状病毒肺炎疫情,热景生物“实验室”1月15日启动研发,20日完成核酸试剂研发,21日开始基因重组蛋白表达,22日开始免疫试剂研发,30日免疫快速试剂和酶免试剂先后研发成功,现在已经研发了三款针对此次病毒的检测试剂盒。
西陇科学
1月27日,控股子公司山东艾克韦生物技术有限公司研发的2019新型冠状病毒核酸检测试剂盒已通过省器械检验中心检测,成为山东省法定检验机构检定合格的首个新型冠状病毒检测产品。在获得国家药监局的上市批件后,这种试剂盒将被发往各地医院,用于测定疑似患者的样本中是否有新型冠状病毒。目前,公司已启动紧急恢复生产预案,定单能保证供应。
迪安诊断
近日已完成新型冠状病毒系列检测试剂新品的研发。产品是基于荧光PCR平台的新型冠状病毒核酸检测试剂盒,目前已经完成在浙江省医疗器械检验研究院的试剂盒注册检验,预计很快能够为市场提供精准检测产品。
美康生物
公司研发的新型冠状病毒核酸检测试剂盒(荧光PCR法)和新型冠状病毒蛋白快速检测试剂盒(免疫层析法)已经处于临床验证阶段。公司称,验证结果符合相关检测标准后,将提交样品及相关资料向国家药品监督管理局进行注册申请。
万孚生物
公司于近日完成新型冠状病毒系列检测试剂新品的研发。该系列产品包括基于胶体金免疫层析法的2019-nCoV新型冠状病毒抗原检测试剂、抗体检测试剂,以及基于荧光PCR平台的2019-nCoV新型冠状病毒核酸检测试剂盒。目前部分产品已经完成了注册产品抽样工作,公司预计很快能为市场提供现场快速检测和精准检测的系列产品。
透景生命
近日已完成新型冠状病毒检测产品的研制,该产品采用的是卡式荧光PCR法,所有的PCR提取、配制和扩增均微缩至一个卡盒内,样本加入卡盒后检测过程全程封闭,将可能的交叉污染和病源传播风险都控制在卡盒内,在提高检测精准度的同时提高了检验人员的安全性。产品实现随机上样,可在床旁或其他开放性实验室即时检测,1-1.5小时后即可出结果。目前,公司正组织人员进行产品的临床验证和注册申报工作。
艾德生物
目前已成功研制出新型冠状病毒基因检测试剂盒(荧光PCR法),操作简单、方便、准确,可以在2小时内获得检测结果,正在申请进入国家药监局为此次疫情开辟的应急审批通道。
嘉兴雅康博医学检验所
嘉兴雅康博医学检验所已开展应对新型冠状病毒感染的检测试剂研发。在北京、嘉兴两地技术团队的通力协作下,团队研发出新型冠状病毒快速检测试剂盒,接下来通过临床试验、注册审批等流程后,即可批量生产投放市场。
康华生物
潍坊市康华生物技术有限公司近日成功研制出新型冠状病毒(2019-nCoV)IgM抗体检测试剂盒(胶体金法)和新型冠状病毒(2019-nCoV)IgM抗体检测试剂盒(免疫层析法)。该产品于2020年1月31日首个通过国家注册检验,目前正在向国家药监局申请应急审批,待取得注册证后,就能投入市场销售。该试剂量产后可达每天50万人份。
贝瑞基因
日前,贝瑞基因“新冠病毒核酸检测专项攻关小组”宣布成功研发新型冠状病毒2019-nCoV核酸变异检测试剂盒(单分子测序法)。基于第三代单分子测序技术平台,该试剂盒可有效检测新冠病毒的核酸序列变异情况,及时掌握病毒变异动态,提升检测的灵敏度,降低病毒核酸检测中因病毒变异产生的“假阴性率”。
新型冠状病毒核酸检测试剂日产量已达77.3万人份
据光明日报消息,2月3日,国务院应对新型冠状病毒感染的肺炎疫情联防联控机制举行新闻发布会,工业和信息化部党组成员、总工程师田玉龙先生表示,到2月1日,新型冠状病毒核酸检测试剂日产量已经达到了77.3万人份,相当于疑似患病者的40倍,从总的供应来看,已经基本满足要求。
田玉龙指出,关于检测试剂的问题,核酸检测试剂是一种很成熟的传染病检测手段,目前是卫生系统和医院直接从企业采购,这个试剂盒理论上讲应该是没有保供的问题,当然因为前期的时间问题、复产的问题,出现了一些小的困难。但目前来看,产能已经恢复。到2月1日,我们日产量已经达到了77.3万人份,相当于疑似患病者的40倍,从总的供应来看,已经基本满足要求了。当然,产能还没有完全恢复,只达到了百分之六七十,后续的工作主要还是恢复产能。
广证恒生指出,短期来看,对于体外诊断试剂盒企业而言,一方面激增的检测刚需将为部分率先获批企业带来直接的业绩与增长,另一方面对于待获批的企业,研发及拿证能力强的企业有望分一杯羹,此外这类企业争取尽快拿证的同时应保证产品质量。
不论如何,产品质量都是至关重要的。此外,结合当前公布的产量,各产品之间的差异如谁能诊断更精准、出结果更快等,占据优势者才是王者。
关键词:试剂盒
分享至:
![]()
![]()




鄂公网安备 42011102004299号
© 2014-2025 前衍化学科技(武汉)有限公司 版权所有 鄂ICP备20009754号-1